Ruta de l'àcid shikímic
La ruta de l'àcid shikímic o via del shikimat, és una ruta metabòlica de set passos usada per bacteris, fongs, algues, paràsits i plantes per la biosíntesi d'aminoàcids aromàtics (fenilalanina, tirosina, i triptòfan). Aquesta ruta metabòlica no es presenta en animals i per tant, els aminoàcids essencials en els animals s'han d'obtenir de la dieta.
Aquesta via no es troba en animals i humans. Els animals i els humans necessiten aquests aminoàcids. D'aquí que els productes d'aquesta via representin aminoàcids essencials. S'han d'obtenir a partir d'organismes que no són animals; o bé, d'animals que la dieta inclou organismes inferiors que tinguin la via shikimat i puguin fer aquests aminoàcids.
Els set enzims implicats en la ruta del shikimat són la DAHP sintasa, la sintasa de 3-deshidroquinata, deshidratasa 3-deshidroquinato, siquimato deshidrogenasa, siquimato cinasa, EPSP sintasa i corismato sintasa. La via s'inicia amb dos substrats, piruvat de fosfenol i eritrosi-4-fosfat i acaba amb corismat, un substrat dels tres aminoàcids aromàtics. El cinquè enzim involucrat és el shikimat kinase, un enzim que catalitza la fosforilació dependent de ATP del shikimat per formar 3-fosfat shikimat (mostrat a la figura següent).[1] El 3-fosfat shikimat s'acobla amb piruvat de fosfenol per donar 5-enolpyruvylshikimat-3-fosfat mitjançant l'enzim 5-enolpyruvylshikimat-3-fosfat (EPSP) sintasa .
A continuació, el 5-enolpyruvylshikimat-3-fosfat es transforma en corismat mitjançant un chorismate sintasa .
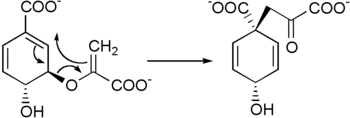
L'àcid prefènic es sintetitza a continuació mitjançant una reordenació de clorisat de Claisen per mutasa corismàtica.[2][3]
El prefenat es descarboxila oxidativament amb la retenció del grup hidroxil per donar <i id="mwRA">p-</i> hidroxifenilpruvat, que es transamina amb glutamat com a font de nitrogen per donar tirosina i α-cetoglutarat .
Referències
[modifica]- ↑ Herrmann, K. M.; Weaver, L. M. Annual Review of Plant Physiology and Plant Molecular Biology, 50, 1999, pàg. 473–503. DOI: 10.1146/annurev.arplant.50.1.473. PMID: 15012217.
- ↑ Helmut Goerisch Biochemistry, 17, 18, 1978, pàg. 3700. DOI: 10.1021/bi00611a004.
- ↑ Peter Kast, Yadu B. Tewari, Olaf Wiest, Donald Hilvert, Kendall N. Houk, and Robert N. Goldberg J. Phys. Chem. B, 101, 50, 1997, pàg. 10976–10982. DOI: 10.1021/jp972501l.
Bibliografia
[modifica]- Edwin Haslam. Shikimic Acid: Metabolism and Metabolites (1st Edition), 1993.
- Brown, Stewart A.; Neish, A. C. Nature, 175, 4459, 1955, pàg. 688–689. DOI: 10.1038/175688a0. ISSN: 0028-0836.
- Weinstein, L. H.; Porter, C. A.; Laurencot, H. J. Nature, 194, 4824, 1962, pàg. 205–206. DOI: 10.1038/194205a0. ISSN: 0028-0836.
- Wilson, D J; Patton, S; Florova, G; Hale, V; Reynolds, K A Journal of Industrial Microbiology and Biotechnology, 20, 5, 1998, pàg. 299–303. DOI: 10.1038/sj.jim.2900527. ISSN: 1367-5435.