Indium(III)-hydroxid
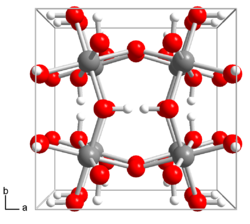
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| _ In3+ _ O2− _ H+ | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Indium(III)-hydroxid | ||||||||||||||||||
| Andere Namen |
Indiumtrihydroxid | ||||||||||||||||||
| Verhältnisformel | In(OH)3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis gelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 165,84 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||||||||
| Dichte |
4,45 g·cm−3 (20 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr wenig löslich in Wasser[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Indium(III)-hydroxid ist eine anorganische chemische Verbindung des Indiums aus der Gruppe der Hydroxide.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Indium(III)-hydroxid kommt natürlich in Form des Minerals Dzhalindit vor.[5]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Indium(III)-hydroxid kann durch Reaktion einer Indium(III)-chlorid-Lösung mit einer Ammoniak-Lösung bei 100 °C und anschließender Trocknung gewonnen werden[6]:
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Indium(III)-hydroxid ist ein weißer bis gelber Feststoff, der eine Kristallstruktur ähnlich dem Rhenium(VI)-oxid-Typ besitzt (Raumgruppe Im3 (Raumgruppen-Nr. 204), Gitterparameter a = 7,974 Å)[7] und sich bei 150 °C durch Wasserabgabe zersetzt.[1][6] Die Verbindung ist wie Aluminiumhydroxid und Gallium(III)-hydroxid amphoter und löst sich in Säuren leichter als in Basen unter Bildung von Indiumsalzen und Indaten. Bei 10 MPa Druck und einer Temperatur von 250 °C bis 400 °C wandelt sie sich in Indiumoxidhydroxid (InO(OH)) um.[8]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Indium(III)-hydroxid kann in der organischen Chemie als Katalysator verwendet werden.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. CRC Press, 2011, ISBN 1-4398-1462-7, S. 208 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Datenblatt Indium(III) hydroxide, 99.99% trace metals basis bei Sigma-Aldrich, abgerufen am 21. März 2014 (PDF).
- ↑ A.J. Downs: Chemistry of Aluminium, Gallium, Indium, and Thallium. Springer, 1993, ISBN 0-7514-0103-X, S. 141 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Eintrag zu Indium(III)-hydroxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Mineralienatlas: Dzhalindit, abgerufen am 22. März 2014.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 870.
- ↑ D.F. Mullica, G.W. Beall, W.O. Milligan, J.D. Korp, I. Bernal: The crystal structure of cubic In(OH)3 by X-Ray and neutron diffraction methods. In: Journal of Inorganic and Nuclear Chemistry, 41, 1979, S. 277–282, doi:10.1016/0022-1902(79)80133-5.
- ↑ Egon Wiberg, Nils Wiberg: Inorganic Chemistry. Academic Press, 2001, ISBN 0-12-352651-5, S. 1034 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Yoshiyuki Onishi, Daigo Ogawa, Makoto Yasuda, Akio Baba: Direct Conversion of Carbonyl Compounds into Organic Halides: Indium(III) Hydroxide-Catalyzed Deoxygenative Halogenation Using Chlorodimethylsilane. In: Journal of the American Chemical Society. 124, 2002, S. 13690–13691, doi:10.1021/ja0283246.
