Putrescyna
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||||
| Wzór sumaryczny |
C4H12N2 | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
NH2(CH2)4NH2 | ||||||||||||||||||||||||||
| Masa molowa |
88,15 g/mol | ||||||||||||||||||||||||||
| Wygląd |
białe, silnie higroskopijne ciało stałe lub bezbarwna ciecz o silnym zapachu podobnym do piperydyny[1] | ||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||
| DrugBank | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||||
Putrescyna[a], 1,4-diaminobutan – organiczny związek chemiczny, amina biogenna z grupy ptomain.
Putrescyna i kadaweryna zostały po raz pierwszy opisane przez lekarza Ludwiga Briegera w Berlinie w 1885 roku. Występuje w bardzo małych ilościach w moczu i ślinie, w której najwyższe stężenie osiąga zaraz po przebudzeniu[potrzebny przypis].
Bierze udział w biosyntezie poliamin[6][7] (spermidyny i sperminy)[8].
Powstawanie
[edytuj | edytuj kod]Powstaje w wyniku rozpadu białek np. gnicia przy udziale bakterii beztlenowych. Odpowiada za nieprzyjemny zapach rozkładającej się materii organicznej (mięsa, tkanek, zwłok) oraz za nieświeży oddech[potrzebny przypis].
Biosynteza
[edytuj | edytuj kod]W organizmach żywych putrescyna powstaje z L-argininy na dwóch ścieżkach: poprzez ornitynę lub agmatynę[9].
Biosynteza przez ornitynę
[edytuj | edytuj kod]Ścieżka ta jest powszechna w świecie żywym[6][10][7]. L-Ornityna powstaje z L-argininy w wyniku hydrolizy katalizowanej przez arginazę (EC 3.5.3.1[11]):
Ornityna ulega następnie dekarboksylacji katalizowanej przez dekarboksylazę ornityny (ODC, EC 4.1.1.17[12]) w obecności fosforanu pirydoksalu[6][10][7]:
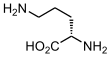 ⇌
⇌ 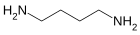 + CO
+ CO
2
Biosynteza przez agmatynę
[edytuj | edytuj kod]Drugą ścieżką syntezy putrescyny, dominującą u roślin wyższych i spotykaną też u niektórych bakterii, jest dekarboksylacja argininy do agmatyny, z udziałem dekarboksylazy argininy (ADC, EC 4.1.1.19[13])[6][14]:
Następnie deiminaza agmatyny (EC 3.5.3.12[15]) przekształca agmatynę w N-karbamoiloputrescynę[6][14]:
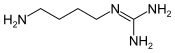 + H
+ H
2O ⇌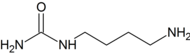 + NH
+ NH
3
Ostatnim etapem jest hydroliza grupy karbamoilowej przez amidazę N-karbamoiloputrescyny (EC 3.5.1.53[16])[6][14]:
Agmatyna może też ulegać bezpośredniej hydrolizie do putrescyny i mocznika. Reakcję tę katalizuje agmantynaza (EC 3.5.3.11[17]), enzym powszechnie występujący u różnych organizmów[18]:
Produkcja i zastosowanie
[edytuj | edytuj kod]Putrescyna produkowana na skalę przemysłową jest surowcem do produkcji leków, środków ochrony roślin i polimerów. Reaguje z kwasem adypinowym do poliamidu nylon-4,6, który jest wprowadzony do obrotu przez koncern DSM pod nazwą handlową Stanyl[potrzebny przypis].
Toksyczność
[edytuj | edytuj kod]Putrescyna jest toksyczna w dużych dawkach. Dawka śmiertelna (LD50) dla zwierząt wynosi 0,5–1,6 g/kg przy podaniu doustnym[4].
Zobacz też
[edytuj | edytuj kod]Uwagi
[edytuj | edytuj kod]Przypisy
[edytuj | edytuj kod]- ↑ a b c d e f g 1,4-Diaminobutane, [w:] PubChem [online], United States National Library of Medicine, CID: 1045 [dostęp 2022-07-19] (ang.).
- ↑ a b c David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 3-72, ISBN 978-1-4200-9084-0 (ang.).
- ↑ Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- ↑ a b c Putrescyna (nr 32790) w katalogu produktów Sigma-Aldrich (Merck). [dostęp 2022-07-19].
- ↑ Putrescine, [w:] ChemIDplus [online], United States National Library of Medicine [dostęp 2022-07-19] (ang.).
- ↑ a b c d e f Colin Hanfrey i inni, Arabidopsis polyamine biosynthesis: absence of ornithine decarboxylase and the mechanism of arginine decarboxylase activity, „The Plant Journal: For Cell and Molecular Biology”, 27 (6), 2001, s. 551–560, DOI: 10.1046/j.1365-313x.2001.01100.x, PMID: 11576438 [dostęp 2022-07-19] (ang.).
- ↑ a b c Andrew D. Kern i inni, Structure of mammalian ornithine decarboxylase at 1.6 A resolution: stereochemical implications of PLP-dependent amino acid decarboxylases, „Structure (London, England: 1993)”, 7 (5), 1999, s. 567–581, DOI: 10.1016/s0969-2126(99)80073-2, PMID: 10378276 [dostęp 2022-07-19] (ang.).
- ↑ Putrescine biosynthesis I, [w:] MetaCyc [online], SRI International [dostęp 2022-07-19].
- ↑ Superpathway of putrescine biosynthesis, [w:] MetaCyc [online], SRI International [dostęp 2022-07-19].
- ↑ a b Wolfgang Legrum, Riechstoffe, zwischen Gestank und Duft, wyd. 1. Aufl, Wiesbaden: Vieweg + Teubner Verlag, 2011, s. 65, ISBN 978-3-8348-1245-2, OCLC 754219016.
- ↑ EC 3.5.3.1 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ EC 4.1.1.17 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ EC 4.1.1.19 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ a b c K.S. Srivenugopal, P.R. Adiga, Enzymic conversion of agmatine to putrescine in Lathyrus sativus seedlings. Purification and properties of a multifunctional enzyme (putrescine synthase), „Journal of Biological Chemistry”, 256 (18), 1981, s. 9532–9541, DOI: 10.1016/S0021-9258(19)68795-8, PMID: 6895223 [dostęp 2022-07-19] (ang.).
- ↑ EC 3.5.3.12 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ EC 3.5.1.53 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ EC 3.5.3.11 [online], Międzynarodowa Unia Biochemii i Biologii Molekularnej [dostęp 2022-07-19] (ang.).
- ↑ Iva Chitrakar i inni, Structure of the E. coli agmatinase, SPEB, „PLOS One”, 16 (4), 2021, art. nr e0248991, DOI: 10.1371/journal.pone.0248991, PMID: 33857156, PMCID: PMC8049259 [dostęp 2022-07-19] (ang.).


