异喹啉
| 异喹啉 | |
|---|---|

| |

| |
| IUPAC名 Isoquinoline | |
| 别名 | 苯并[c]吡啶 |
| 识别 | |
| CAS号 | 119-65-3 |
| PubChem | 8405 |
| ChemSpider | 8098 |
| SMILES |
|
| InChI |
|
| InChIKey | AWJUIBRHMBBTKR-UHFFFAOYAX |
| EINECS | 204-341-8 |
| ChEBI | 16092 |
| DrugBank | DB04329 |
| 性质 | |
| 化学式 | C9H7N |
| 摩尔质量 | 129.16 g·mol⁻¹ |
| 外观 | 无色片状低熔点固体 |
| 密度 | 1.099 g/cm³ |
| 熔点 | 26~28 °C |
| 沸点 | 242 °C |
| 溶解性(水) | 微溶于水 |
| 蒸氣壓 | 5 Pa (20°C) |
| 折光度n D |
1.62078 (30°C) |
| 危险性 | |
| 欧盟危险性符号 | |
| 警示术语 | R:R22, R24 |
| 安全术语 | S:S24/25, S36/37, S45 |
| 闪点 | 107 °C |
| 致死量或浓度: | |
LD50(中位剂量)
|
360 mg/kg(大鼠,口服)[1] 180 mg/kg(大鼠,皮肤) |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
异喹啉(英語:Isoquinoline)是由萘中的一个 β-CH 基团被氮替换衍生出来的杂环化合物,与喹啉互为同分异构体,有芳香性。
物理性质
[编辑]异喹啉是无色低熔点片状结晶、固体或液体,有类似茴香油和苯甲醛混合物的香味,通常存放后颜色会发黄。存在于煤焦油和骨油中。微溶于水,溶于稀酸,能与多种有机溶剂混溶。能随水蒸气蒸发。具吸水性。有碱性,pKa = 5.4,碱性较喹啉强,比吡啶略强,能与各种酸成盐,其盐酸盐熔点 209°C。
历史
[编辑]1885年 Hoogewerff 和 van Dorp[2]从煤焦油喹啉馏分中用分级结晶法获得了硫酸异喹啉。同年 Gabriel[3]完成了异喹啉的合成。1914年 Weißgerber[4]利用异喹啉和喹啉之间的碱性差异,发展了一种更为有效的分离方法。
生产
[编辑]工业上主要以煤焦油粗喹啉馏分为原料,通过磺化、分级结晶、过滤、重结晶、氨水分解、洗涤和精馏生产异喹啉。
化学性质
[编辑]异喹啉的化学性质与吡啶和喹啉相似,质子化、烷基化、酰化以及被过氧酸氧化都在 N 原子上进行,亲电芳香取代和亲核芳香取代反应主要在环上的 C 原子上进行。
取代反应
[编辑]异喹啉的亲电芳香取代活性高于吡啶,优先发生在异喹啉环的 5- 和 8-位,以 5-位产物为主。[5][6]通过N-质子化进行苯环上C-质子化然后进行质子交换,需要硫酸这样的强酸,而且反应在 C-5 上比 C-8 上快。[7]亲核芳香取代在异喹啉的杂环进行,优先发生在 1-位。例如,异喹啉经过 Chichibabin反应可得1-氨基异喹啉;[8]与正丁基锂发生 Ziegler反应得到1-正丁基异喹啉,这个反应的一级加成产物1-正丁基-1,2-二氢异喹啉受稠合苯环的影响而得到稳定,可被分离出来,经硝基苯氧化可在碳上取代,并恢复异喹啉环的芳香性。
异喹啉可以在高温下通入氢气流与氢氧化钾反应而直接羟基化,产物是1-异喹啉酮。[9]
异喹啉 3-位的卤素表现出与卤代苯相似的性质,但 1-位的卤素具有与 α- 和 γ-卤代吡啶相似的敏感性,很容易发生亲核芳香取代。例如,1,3-二氯异喹啉可选择性地被甲氧基取代为 1-甲氧基-3-氯异喹啉。然而,3-卤代异喹啉惰性的一个明显例外是 3-溴代异喹啉与氨基钠通过ANRORC机理发生的取代反应,在这个反应中环氮原子变为取代基上的氮原子,生成3-氨基异喹啉。[10]
异喹啉在苯甲酰氯等酰化试剂的作用下,与氰化钾或三甲基氰硅烷发生 Reissert反应,生成 Reissert 化合物 2-酰基-1-氰基-1,2-二氢异喹啉。Reissert 化合物可以发生一系列在合成上有用的转换。[11][12]
异喹啉可以与过氧化苯甲酰作用,生成多种苯基异喹啉的混合物。如果用异喹啉正离子为作用物,则可通过它在酸性溶液中与亲核性更强的自由基的取代反应,在异喹啉的 1-位引入酰基和酰胺基。
氧化还原反应
[编辑]异喹啉被碱性高锰酸钾氧化,两个环都可被降解,得到的是吡啶-3,4-二甲酸和邻苯二甲酸的混合物。[13]而在中性介质中用高锰酸钾氧化,不氧化苯环,只生成邻苯二甲酰亚胺。苯环上的取代基可以影响氧化反应的结果。
异喹啉可以被催化氢化、氢化试剂或金属还原;也可以实现选择性完全还原或部分还原异喹啉的吡啶环或苯环。催化氢化的产物受反应介质酸性的影响很大:在乙酸中,吡啶环选择性还原生成1,2,3,4-四氢异喹啉;而在浓盐酸中,苯环被选择性还原生成5,6,7,8-四氢异喹啉,进一步还原则生成顺式和反式十氢异喹啉的混合物。
异喹啉用二乙基氢化铝或氢化铝锂[14]还原可以得到很活泼的1,2-二氢异喹啉;在液氨中用锂还原则得到3,4-二氢异喹啉[15]。异喹啉鎓离子被质子溶剂中的硼氢化钠迅速还原生成1,2,3,4-四氢异喹啉,该反应是确定生物碱结构的一个重要反应。杂环部分迅速被还原,其它可被还原的官能团如羰基可以不受影响。
其他反应
[编辑]异喹啉杂环上的甲基具有 CH 酸性,1-位甲基氢酸性大于3-位,因此能够发生酸或碱催化的 C-C 键形成反应。
异喹啉鎓盐中的吡啶鎓环较容易进行亲核加成,可与富电子的亲双烯体如乙烯基乙醚发生环加成反应。[16]
合成
[编辑]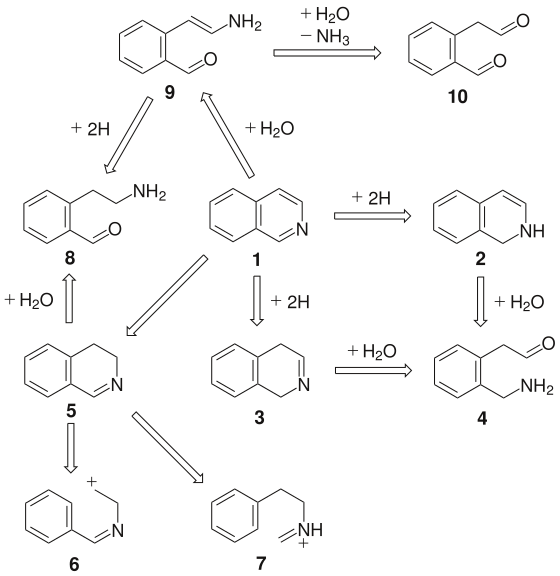
从异喹啉 1 的逆合成分析可以看出,如果从亚胺键的断裂回推,可以通过二羰基化合物 10 作为环合原料。如果算上还原步骤,可用氨基羰基化合物 8 和 4 作为二氢异喹啉的制取原料。另一方面,3,4-二氢异喹啉 5 的 C-1 和 C-4 键断裂可以产生合成子 α-亲电性烯胺 7 以及 β-亲电性烯胺 6,它们也可用作亲电芳香取代环化的原料。
因此,异喹啉及其衍生物的合成方法有:
1、(2-甲酰苯基)乙醛及类似的二羰基化合物与氨发生环化反应生成异喹啉(合成子 10)。如果用羟胺、肼或伯胺代替氨,则可分别得到异喹啉N-氧化物、N-内铵盐和N-取代的异喹啉鎓离子。
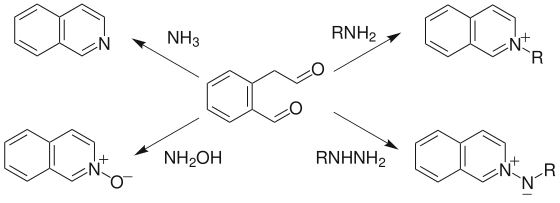
2、Bischler-Napieralski反应:2-芳基乙胺与酰氯或酸酐反应生成酰胺,然后在失水剂作用下环化生成3,4-二氢异喹啉,然后脱氢生成1-取代的异喹啉(合成子 7)。
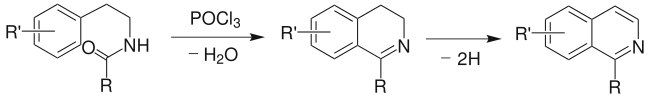
Pictet-Gams反应:上述反应的改进法,用 β-甲氧基或 β-羟基芳乙胺进行反应,可不经氧化或脱氢,直接得到异喹啉类化合物。反应中有噁唑啉中间体生成。
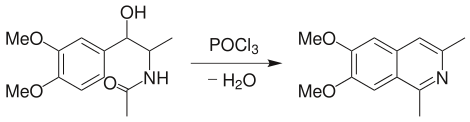
3、Pictet-Spengler反应:2-芳基乙胺与醛在酸催化下生成亚胺,然后亚胺在酸催化下环化生成1,2,3,4-四氢异喹啉,脱氢得到异喹啉(合成子 7)。
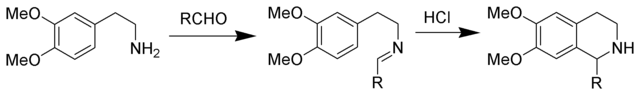
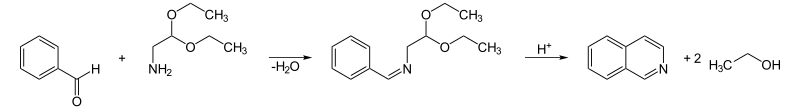
4、Pomeranz-Fritsch合成:芳醛与氨基乙缩醛缩合生成亚胺,亚胺在酸催化下环化为杂环上无取代基的异喹啉(合成子 6)。
用途
[编辑]用作合成药物、染料、杀虫剂的中间体及气相色谱固定液。
异喹啉衍生物广泛存在于自然界中,[17]目前已知的异喹啉生物碱有1000多种,是已知生物碱中最大的一类。它们多以异喹啉或四氢异喹啉为母核,又可根据连接基团而细分为异喹啉类、苄基异喹啉类、双苄基异喹啉类、阿扑芬类、原小檗碱类、普罗托品类、吐根碱类、α-萘菲啶类和吗啡类生物碱等九类。
有许多药物是异喹啉的衍生物。著名的异喹啉类生物碱罂粟碱,至今仍是重要的解痉药。抗抑郁药诺米芬辛和抗血吸虫药吡喹酮是从四氢异喹啉衍生而来。
内文注释
[编辑]- ^ Smyth et al., Arch. Ind. Hyg. Occup. Med. 4, 119 (1951)
- ^ S. Hoogewerff and W. A. van Dorp, Rec. Trav. Chim. Pays-Bas, 4, 125 (1885).
- ^ S. Gabriel. Synthese von Derivaten des Isochinolins. Berichte der deutschen chemischen Gesellschaft. 1885, 18 (2): 3470–3480. doi:10.1002/cber.188501802334.
- ^ R. Weißgerber. Über das Isochinolin im Steinkohlenteer. Berichte der deutschen chemischen Gesellschaft. 1914, 47 (3): 3175–3181. doi:10.1002/cber.191404703123.
- ^ M. J. S. Dewar and P. M. Maitlis. Electrophilic substitution. Part XI. Nitration of some six-membered nitrogen-heterocyclic compounds in sulphuric acid. J. Chem. Soc. 1957: 2521–2528. doi:10.1039/JR9570002521.
- ^ J. A. Beisler. A short synthesis of several gambir alkaloids. Tetrahedron. 1970, 26 (8): 1961–1965. doi:10.1016/S0040-4020(01)92772-3.
- ^ U. Bressel, A. R. Katritzky and J. R. Lea. Kinetics and mechanism of electrophilic substitution of heteroaromatic compounds. Part XXIII. Acid-catalysed hydrogen exchange of quinoline, isoquinoline, and their N-oxides. J. Chem. Soc. (B). 1971: 4–10. doi:10.1039/J29710000004.
- ^ F. W. Bergstrom. Die direkte Einführung von Aminogruppen in den aromatischen und heterocyclischen Ring. II. Die Reaktion von Iso-chinolin mit Alkali- und Erdalkali-amiden in flüssigem Ammoniak. Justus Liebigs Ann. Chem. 1935, 515 (1): 34–42. doi:10.1002/jlac.19355150105.
- ^ Jan J. M. Vandewalle, Ernest de Ruiter, Hans Reimlinger, René A. Lenaers. Notiz über eine verbesserte Darstellung von Isocarbostyril und Carbostyril. Chemische Berichte. 1975, 108 (12): 3898–3899. doi:10.1002/cber.19751081223.
- ^ Sanders, G. M., van Dijk, M., and den Hertog, H. J., Recl. Trav. Chim. Pays-Bas, 93, 198 (1974).
- ^ Frank D. Popp, John M. Wefer. Reissert compound studies. XV. preparation and reaction of the reissert anion at room temperature. J. Heterocycl. Chem. 1967, 4 (2): 183–187. doi:10.1002/jhet.5570040204.
- ^ Jung-Tai Hahn, Joydeep Kant, Frank D. Popp, Siri Ram Chhabra, Barrie C. Uff. Reissert compound studies. LXV. Preparation of reissert compounds derived from α,β-unsaturated acid chlorides. J. Heterocycl. Chem. 1992, 29 (5): 1165–1176. doi:10.1002/jhet.5570290521.
- ^ S. Hoogewerff, W. A. van Dorp. Sur les Produits de l'oxydation de l'isoquinoléine par le permanganate de potassium. Rec. Trav. Chim. Pays-Bas. 1885, 4: 285–293.
- ^ Jackman, L. M. and Packham, D. I., Chem. Ind. (London), 1955, 360.
- ^ Walter Hückel, Gerhard Graner. Reduktionen in flüssigem Ammoniak, XI. Isochinolin. Chemische Berichte. 1957, 90 (9): 2017–2023. doi:10.1002/cber.19570900945.
- ^ F. Howard Day, Charles K. Bradsher, Teh-Kuei Chen. Cycloaddition reactions of some 5-substituted isoquinolinium salts. J. Org. Chem. 1975, 40 (9): 1195–1198. doi:10.1021/jo00897a002.
- ^ Hesse, Manfred. Alkaloide 1st ed. Weinheim: Wiley-VHC. 2000. ISBN 978-3-906390-19-2.
参考资料
[编辑]- T. Eicher, S. Hauptmann 著,李润涛、葛泽梅、王欣 译. 杂环化学——结构、反应、合成与应用(The Chemistry of Heterocycles: Structures, Reactions, Synthesis and Applications) 第二版. 北京: 化学工业出版社. 2005年11月: 287–298. ISBN 7-5025-7960-5.
- J. A. Joule, K. Mills 著,由业诚、高大彬等译. 杂环化学(Heterocyclic Chemistry) 4th ed. 北京: 科学出版社. 2004年7月: 131–163. ISBN 7-03-012736-6.
- 陈敏为,甘礼骓. 有机杂环化合物 第一版. 北京: 高等教育出版社. 1990年6月: 102–119. ISBN 7-04-001122-0.
- T. Kametani, Edited by John ApSimon. The Total Synthesis of Isoquinoline Alkaloids. from "The Total Synthesis of Natural Products", Volume 3. Toronto: John Wiley & Sons, Inc. 1977: 3–251. ISBN 0-471-02392-2.
- 徐仁生主编,叶阳、赵维民副主编. 《天然产物化学》(第二版). 北京: 科学出版社. 2004年9月: 115–127. ISBN 7-03-012518-5.
