Bromuro di acetile
| Bromuro di acetile | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C2H3BrO |
| Massa molecolare (u) | 122,95 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 208-061-7 |
| PubChem | 10482 |
| SMILES | CC(=O)Br |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | 1,65[1] |
| Indice di rifrazione | 1,4486[2] |
| Solubilità in acqua | reagisce violentemente |
| Temperatura di fusione | –96 °C[1] |
| Temperatura di ebollizione | 76,7 °C[1] |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | –223,5[2] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 290 - 314 - EUH014 [1] |
| Consigli P | 234 - 280 - 301+330+331 - 303+361+353 - 304+340+310 - 305+351+338 [1] |
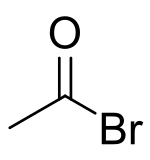
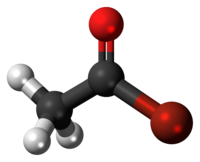
Il bromuro di acetile è un alogenuro acilico di formula CH3C(O)Br. Questo organobromuro è un liquido incolore fumante di odore pungente, formalmente derivato dell'acido acetico sostituendo l'ossidrile con un atomo di bromo. Viene usato principalmente come acetilante in sintesi organica.[3]
Sintesi
[modifica | modifica wikitesto]Il bromuro di acetile fu sintetizzato per la prima volta nel 1863 dal chimico francese Henri Gal (1839-1898), distillandolo da una miscela di acido acetico, bromo e fosforo.[4] In laboratorio si può sintetizzare per reazione tra acido acetico e tribromuro di fosforo:[5]
- 3CH3COOH + PBr3 → 3CH3COBr + H3PO3
Reattività
[modifica | modifica wikitesto]Il bromuro di acetile puro è un liquido incolore, ma i prodotti commerciali sono spesso giallo-bruni per la presenza di bromo formato per decomposizione.
Analogamente agli altri alogenuri di acetile, anche il bromuro di acetile reagisce a contatto con l'acqua. In questo caso si formano acido bromidrico e acido acetico:
- CH3COBr + H2O → HBr + CH3COOH
Tossicità / indicazioni di sicurezza
[modifica | modifica wikitesto]Il bromuro di acetile è disponibile in commercio. Il composto è corrosivo, e provoca ustioni agli occhi, alla pelle e alle mucose. Reagisce violentemente con acqua e umidità producendo acido bromidrico. Non è classificato come cancerogeno. È nocivo per gli organismi acquatici.[6]
Note
[modifica | modifica wikitesto]Bibliografia
[modifica | modifica wikitesto]- (EN) Th. M. Burton e Ed. F. Degering, The Preparation of Acetyl Bromide, in J. Am. Chem. Soc., vol. 62, n. 1, 1940, pp. 227–227, DOI:10.1021/ja01858a502.
- (DE) H. Gal, Ueber die Einwirkung des Broms auf Bromacetyl und über die Tribromessigsäure, in Justus Liebigs Annalen der Chemie, vol. 129, n. 1, 1864, pp. 53-57, DOI:10.1002/jlac.18641290107.
- GESTIS, Acetyl bromide, su gestis.dguv.de. URL consultato il 28 agosto 2015. Pagina del bromuro di acetile nel data base GESTIS.
- Acetylbromid, in Lexikon Der Chemie, Spektrum Akademischer Verlag, 1998. URL consultato il 30 agosto 2015.
- D. R. Lide (Editor), CRC Handbook of Chemistry and Physics, Internet Version 2005, su hbcpnetbase.com, CRC Press, Boca Raton, 2005. URL consultato il 7 ottobre 2014 (archiviato dall'url originale il 24 luglio 2017).
- Sigma-Aldrich, Scheda di dati di sicurezza del bromuro di acetile, su sigmaaldrich.com, 2014. URL consultato il 28 agosto 2015.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Bromuro di acetile
Wikimedia Commons contiene immagini o altri file su Bromuro di acetile